B、根据化合物中元素的质量分数=$\frac{相对原子质量×原子个数}{相对分子质量}$×100%,进行分析判断.
D、根据题意,工业上将金属钠于97~100℃熔融,向反应容器中火星电竞首页 火星电竞网站缓慢通入无水液氨(NH3),再加热至一定温度生产氨基钠和氢气,进行分析判断.
解答解:A、钠元素显+1价,氢元素显+1价,设氮元素的化合价是x,根据在化合物中正负化合价代数和为零,可得:(+1)+x+(+1)×2=0,则x=-3价,故选项说法正确.
C、工业上将金属钠于97~100℃熔融,说明钠的熔点本高于97℃,而铁的熔点为1525℃,钠的熔点比铁的熔点低,故选项说法正确.
D、将金属钠于97~100℃熔融,向反应容器中缓慢通入无水液氨(NH3),再加热至一定温度生成氨基钠和氢气,反应的化学方程式为2Na+2NH3$\frac{\underline{\;\;△\;\;}}{\;}$2NaNH2+H2,选项中化学方程式配平错误,故选项说法错误.
点评本题难度不大,理解制取氨基钠的反应原理,掌握化合火星电竞首页 火星电竞网站价的原则、化学式的有关计算等是正确解答本题的关键.
(1)自来水厂常用活性炭来吸附水中的异味和色素;检验自来水是硬水还是软水常用肥皂水.
(2)为了除去水中的杂质,某同学取一定量的河水放入容器中,先加入少量明矾搅拌溶解,静置一段时间,倒入净水器中过滤.加明矾的作用是吸附较大颗粒,加速沉降.
(3)“节约用水,从我做起.”请你任举一例生活中节约用水的具体措施:一水多用,洗菜水浇花、冲厕等.
若证明鸡蛋壳的主要成分是碳酸盐,将A装置的a导气管与C装置的d导气管相连
若A装置中放入稀硫酸和锌粒,用D装置收集干燥氢气,导管口的连接顺序是a→b→c→f
若A装置中放入稀硫酸和锌粒,在D装置中装满水,再连接量筒,气体应从f导管口进入装置D,就可以测定生成氢气的体积
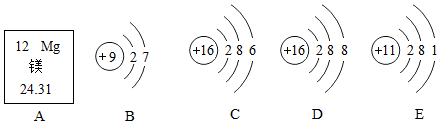
(2)B、C、D、E中属于同种元素的是C和D,原因是质子数(或核电荷数)相等,表示原子的有BCD.
(1)取一只红色的短蜡烛,用小刀切下一小块,把它放入水中,蜡烛一直浮在水面上.据此请总结出常温下蜡烛的两条物理性质:红色固体、不溶于水、密度比水小
(2)点燃蜡烛(图一),能观察到发生化学变化的现象:发光、发热、燃烧等(写出一条)
(3)取一小木条,迅速平放火焰中(图二)约一秒后取出,观察到木条出现环形焦斑.据此推测,蜡烛火焰中外焰温度最高.
(4)将短玻璃导管插入焰心,用燃烧的木条靠近导管另一端(图三),发现导出的气体可以点燃.请你推测,导管里气体可能会是石蜡蒸汽
(5)一只冷而干燥的烧杯罩在蜡烛火焰上方(图四),观察烧杯壁上有水珠出现;片刻后取下烧杯,迅速向烧杯内倒入少量澄清的石灰水,振荡,观察到澄清石灰水变浑浊.由此推断石蜡燃烧后的产物为二氧化碳和水.
